Ein Überblick über Wasserstoffspeicherlegierungen

Anders als physikalische Wasserstoffspeichermethoden wie Hochdruckgasflaschen oder Niedertemperaturverflüssigung können Wasserstoffspeicherlegierungen Wasserstoff durch Kombination mit Hydrierung in Form von Metallhydrid speichern und unter bestimmten Bedingungen Wasserstoff freisetzen. Die Verwendung von Wasserstoffspeicherlegierungen zur Speicherung von Wasserstoff bietet nicht nur die Eigenschaften großer Wasserstoffspeicher, geringen Energieverbrauch und bequemer Verwendung, sondern vermeidet auch den riesigen und sperrigen Stahlbehälter, was die Lagerung und den Transport bequemer und sicherer macht.
Als Wasserstoffspeichermaterial gelten für Legierungen je nach Verwendungszweck unterschiedliche Anforderungen. Generell gibt es mehrere grundlegende Anforderungen: Erstens muss die Wasserstoffabsorptionskapazität pro Massen- und Volumeneinheit groß sein, da dies die verfügbare Energiemenge bestimmt. Zweitens muss der Gleichgewichtsdruck für die Bildung und Zersetzung von Metallhydriden angemessen sein, d. h. sie müssen bei einem geeigneten und stabilen Wasserstoffdruck eine große Menge Wasserstoff absorbieren und freisetzen können. Drittens muss die Wasserstoffabsorptions- und -desorptionsrate schnell und gut reversibel sein. Viertens muss es starke antioxidative, feuchtigkeits- und verunreinigungsvergiftende Eigenschaften haben und eine hohe Zyklenlebensdauer aufweisen. Dies ist wie bei der biologischen Atmung, die ausreichend Atem, ruhiges und gleichmäßiges Atmen erfordert.
Die Erforschung von Wasserstoffspeicherlegierungen begann in den 1960er Jahren. Zunächst entdeckten Reilly und Wiswall vom Brooke-Haven National Laboratory in den USA eine Mg-Wasserstoffspeicher-Ni-Legierung mit einem mg/Ni-Verhältnis von 2:1. 1970 entdeckte das Phillips Laboratory in den Niederlanden die LaNi5-Legierung, die bei Raumtemperatur gute Wasserstoffspeichereigenschaften aufweist. Dann entdeckten Reilly und Wiswall intermetallische FeTi-Verbindungen. Seitdem haben Länder auf der ganzen Welt nie aufgehört, neue Wasserstoffspeicherlegierungen zu erforschen und zu entwickeln.
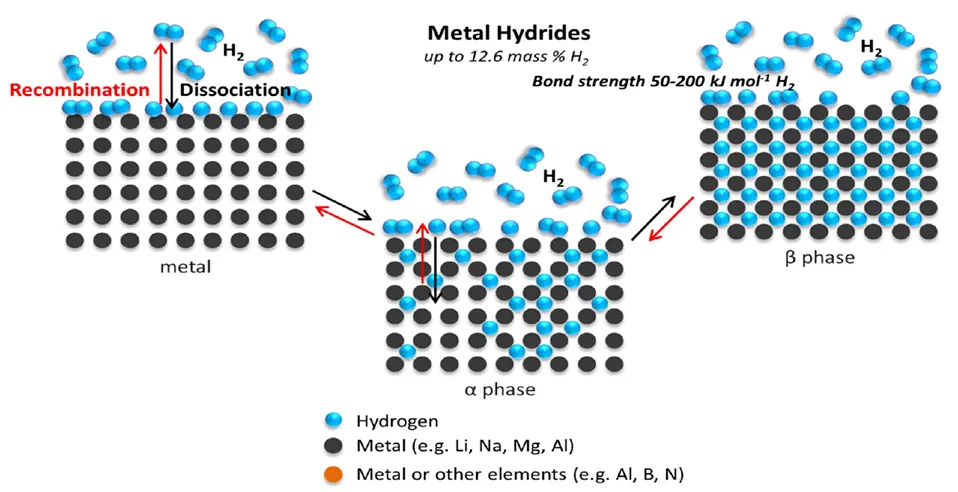
Abbildung 1 Schematische Darstellung des Wasserstoffabsorptionsmechanismus von Wasserstoffspeicherlegierungen
Metallelemente, die mit Wasserstoff reagieren und Hydride bilden können, können im Allgemeinen in zwei Kategorien unterteilt werden: Eine sind Metalle der A-Klasse wie Ti, Zr, Ca, Mg, V, Nb, Seltenerdelemente usw. Diese Metallelemente reagieren leicht mit Wasserstoff zu stabilen Hydriden und setzen dabei eine große Menge Wärme frei. Diese Metalle werden als exotherme Metalle bezeichnet. Eine andere Kategorie sind Metalle der B-Klasse wie Fe, Co, Ni, Cr, Cu, Al usw. Diese Metallelemente haben eine geringe Affinität zu Wasserstoff und bilden nicht leicht Hydride. Wenn sich Wasserstoff in ihnen löst, handelt es sich um eine endotherme Reaktion. Daher werden diese Metalle als endotherme Metalle bezeichnet. Die derzeit erforschten und entwickelten Wasserstoffspeicherlegierungen bestehen hauptsächlich aus Metallen der A-Klasse und Metallen der B-Klasse, um Wasserstoffspeicherlegierungen mit reversibler Wasserstoffabsorptions- und -desorptionsfähigkeit bei geeigneten Temperaturen herzustellen. Diese Wasserstoffspeicherlegierungen können hauptsächlich in die folgenden Kategorien unterteilt werden: Typ AB5 (Seltene Erden), Typ AB₂ (Zirkonium- und Titanreihe), Typ AB (Eisen-Titanreihe), Typ A₂B (Magnesiumreihe) Wasserstoffspeicherlegierungen usw.
Die große Familie der Wasserstoffspeicherlegierungen
(1) Seltenerd-Wasserstoffspeicherlegierung vom Typ AB5
Die Seltenerd-Wasserstoffspeicherlegierung LaNi5 gilt als diejenige mit der besten Anwendungsleistung unter allen Wasserstoffspeicherlegierungen. Ihre Kristallstruktur ist in Abbildung 2 dargestellt. LaNi5 reagiert bei Raumtemperatur bei verschiedenen atmosphärischen Drücken mit Wasserstoff und kann hydriert werden, um LaNi5H6 zu erzeugen. Die Wasserstoffspeicherkapazität beträgt etwa 1,4 Gew.-%, der Zersetzungsdruck (Wasserstofffreisetzungsgleichgewichtsdruck) bei 25 Grad beträgt etwa 0,2 MPa, die Wasserstoffabsorptions- und -freisetzungsrate ist schnell und sie ist sehr gut für die Verwendung in Umgebungen mit Raumtemperatur geeignet. Nach der Absorption von Wasserstoff dehnt sich jedoch das Volumen der Einheitszelle aus (etwa 23,5 %), und bei wiederholter Wasserstoffabsorption und -freisetzung wird die Legierung stark pulverisiert. Seltenerd-AB5-Typ LaNi5 und verwandte Derivatlegierungen können als negative Elektrodenmaterialien für Nickel-Metallhydrid-Batterien verwendet werden und werden mittlerweile in verschiedenen Ländern industriell eingesetzt.
In den letzten Jahren wurden bei Seltenerd-Wasserstoffspeicherlegierungen nichtstöchiometrische AB₃- und A2B7-Wasserstoffspeicherlegierungen entwickelt. Die Wasserstoffspeicherkapazität der Legierung ist höher als die der AB5-Legierung und sie kann Wasserstoff bei Raumtemperatur absorbieren, wie beispielsweise La0.7Mg0.3Ni2. Die reversible Wasserstoffspeicherkapazität von .8Co0.3 kann 1,8 Gew.-% erreichen.
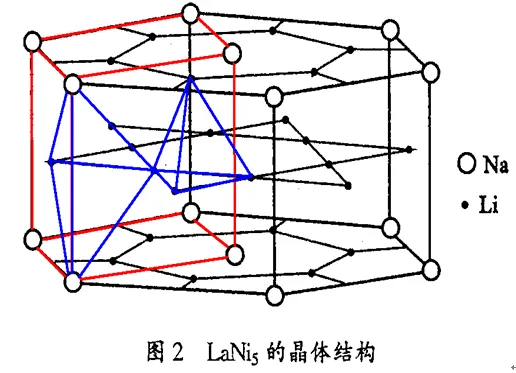
Abbildung 2 Kristallstruktur von LaNi5
(2) AB2-Typ Wasserstoffspeicherlegierungen auf Zirkonium- und Titanbasis
AB₂-Typ Laves-Phase-Wasserstoffspeicherlegierungen werden in zwei Kategorien unterteilt: auf Titanbasis und auf Zirkoniumbasis. Zirkoniumbasierte AB₂-Typ-Wasserstoffspeicherlegierungen umfassen hauptsächlich die Zr-V-Reihe, die Zr-Cr-Reihe und die Zr-Mn-Reihe. ZrMn₂ ist eine Legierung mit einer großen Wasserstoffabsorptionskapazität (Wasserstoffspeicherkapazität 2,0Gew.-%, theoretische elektrochemische Kapazität 482mAh/g). In den späten 1980er Jahren wurde zur Anpassung an die Entwicklung von Elektrodenmaterialien eine Reihe von Elektrodenmaterialien auf Basis von ZrMn-Legierungen entwickelt. Dieser Materialtyp hat die Vorteile einer hohen Entladekapazität und einer guten Aktivierungsleistung, sodass er gute Anwendungsaussichten hat. Titanbasierte AB₂-Typ-Wasserstoffspeicherlegierungen umfassen hauptsächlich zwei Kategorien: auf TiMn-Basis und auf TiCr-Basis. Bei der Optimierung der Ti-Mn-Zusammensetzung stellte die japanische Panasonic Corporation fest, dass die Legierung mit Mn/Ti=1,5 die größte Wasserstoffspeicherkapazität bei Raumtemperatur aufweist, die TiMn1,5H2,5 erreichen kann (Wasserstoffgehalt beträgt etwa 1,8 Gew.-%). Darüber hinaus können Oberflächenmodifikationen wie heiße Alkaliimprägnierung und Fluorierungsbehandlung die Aktivierung und die schnelle Wasserstofflade- und -entladeleistung der Legierung erheblich verbessern.
Titan/Zirkonium-Wasserstoffspeicherlegierungen werden hauptsächlich in Metallhydrid-Wasserstoffspeichertanks von Wasserstoff-Brennstoffzellenfahrzeugen verwendet. Derzeit weisen Legierungen vom Typ AB₂ Probleme auf, wie z. B. Schwierigkeiten bei der Erstaktivierung, schlechte Hochstrom-Entladeleistung und relativ hohe Rohstoffpreise für die Legierungen. Da Legierungen vom Typ AB₂ jedoch die Vorteile einer hohen Wasserstoffspeicherkapazität und einer langen Lebensdauer haben, gelten sie als Nickel-Metallhydrid-Batterien. Die nächste Generation von Anodenmaterialien mit hoher Kapazität.
(3) Eisen-Titan-Wasserstoffspeicherlegierung vom Typ AB
Zu den Wasserstoffspeicherlegierungen vom Typ AB zählen Legierungen auf TiFe-Basis und Legierungen auf TiNi-Basis. Die TiFe-Legierung ist ein typischer Vertreter der Wasserstoffspeicherlegierungen vom Typ AB und wurde 1974 von Reilly und Wiswall vom Brookhaven National Research Institute in den USA entdeckt. Nach der Aktivierung kann die TiFe-Legierung bei Raumtemperatur reversibel eine große Menge Wasserstoff aufnehmen und freisetzen. Die theoretische Wasserstoffspeicherkapazität beträgt 1,6 Gew.-% und der Gleichgewichtswasserstoffdruck bei Raumtemperatur beträgt 7,3 MPa. Sie ist sehr nah an der industriellen Anwendung, ist billig und verfügt über reichlich Ressourcen. Sie wird in der industriellen Produktion weithin verwendet. Sie hat bestimmte Vorteile. Allerdings haben TiFe-Legierungen auch große Nachteile, wie z. B. Schwierigkeiten bei der Aktivierung, geringe Beständigkeit gegen Vergiftung durch Verunreinigungsgase und Leistungseinbußen nach wiederholter Aufnahme und Freisetzung von Wasserstoff. Um diese Mängel zu überwinden und geeignetere Legierungen zu entwickeln, haben die Menschen eine Reihe neuer Legierungen auf Basis von Ti-Fe-Binärlegierungen entwickelt, indem sie Fe durch andere Elemente ersetzt haben.
(4) Magnesium-Wasserstoffspeicherlegierung vom Typ A₂B
Mg steht an achter Stelle in der Erdkruste (2,7 %) und ist in großen Mengen vorhanden. Aufgrund seiner aktiven chemischen Eigenschaften kommt es in der Natur in Form von Verbindungen oder Mineralien vor. Das Atomstrukturmodell der Magnesium-Wasserstoff-Speicherlegierung ist in Abbildung 3 dargestellt. Bei 300 bis 400 Grad und hohem Wasserstoffdruck kann Magnesium direkt mit Wasserstoff reagieren und MgH₂ bilden und eine große Menge Wärme freisetzen. Die Reaktionsgleichung lautet wie folgt:
Mg + H₂=MgH₂
Sein theoretischer Wasserstoffgehalt kann 7,6 Gew.-% H erreichen. Unter den reversiblen Hydriden, die zur Wasserstoffspeicherung verwendet werden, hat Magnesiumhydrid die höchste Energiedichte (9 MJ/kg Mg) und ist ein sehr vielversprechendes Wasserstoffspeichermaterial. Mg hat jedoch eine hohe thermodynamische Stabilität und eine schlechte Wasserstofffreisetzungsleistung. Daher kann reines Magnesium nur bei hohen Temperaturen und hohem Wasserstoffdruck hydriert und bei hohen Temperaturen und niedrigem Druck dehydriert werden, was seine praktische Anwendung einschränkt.
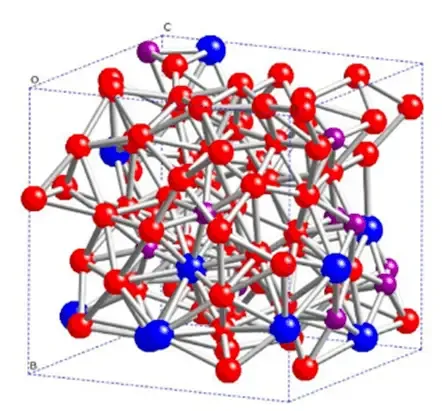
Abbildung 3 Atomstrukturmodell von magnesiumbasierten Wasserstoffspeicherlegierungen
Um die Wasserstofffreisetzungstemperatur von Mg zu senken und die thermodynamischen Eigenschaften zu verbessern, wird Mg mit Ni, Cr, Co, Fe, Ti, RE (Seltene Erden) und anderen Metallen legiert, um binäre oder komplexere Legierungen und Hydride sowie komplexe Hydride herzustellen. Die Zersetzungstemperatur von MgH₂ ist häufig niedriger als die von MgH₂. Nach diesem Konzept entwickelte magnesiumbasierte Wasserstoffspeicherlegierungen umfassen hauptsächlich Mg-Co, Mg-Cu, Mg-Ni, Mg-Fe, Mg-La, Mg-Al und andere Systeme sowie auf dieser Basis entwickelte ternäre und mehrkomponentige Legierungen. Die Verbesserung der Wasserstoffabsorptions- und -desorptionsrate des reinen Mg-H-Wasserstoffspeichersystems kann durch Modifizierung der Oberfläche der Mg-Matrix, Vergrößerung ihrer Oberfläche zur Erhöhung der Affinität der Matrixoberfläche für Wasserstoff und Erhöhung der Diffusionsrate erreicht werden. Unter diesen können Methoden wie das mechanische Kugelmahlen und die Zugabe von Katalysatoren die Wasserstoffabsorptions- und -freisetzungsleistung der Mg-Matrix deutlich verbessern und die Möglichkeit der praktischen Anwendung erhöhen.
HNRE hat eine Vielzahl neuer Wasserstoffspeichermaterialien entwickelt und ein Forschungs- und Entwicklungssystem mit unabhängigen geistigen Eigentumsrechten aufgebaut, das die Anwendung von Wasserstoffspeichermaterialien erforscht, vor allem Seltenerd-Wasserstoffspeicher und hochreine Wasserstoffreinigungs-Seltenerdmaterialien entwickelt und verschiedene wichtige technische Probleme in technischen Anwendungen löst. Ein bestimmtes Wasserstoffspeichermaterial wurde 1998 mit dem zweiten Preis für nationale technische Erfindungen ausgezeichnet. HNRE beliefert Kunden im In- und Ausland mit allen Arten von Wasserstoffspeichermaterialien, insbesondere LaNi- und MgNi-Legierungen.
